近年来,随着免疫疗法作为癌症患者的潜在突破而日益突出,研究人员已经转向了一系列生物标志物分析方法,包括蛋白质组学研究,以帮助解释对这些药物的反应率的变化。
免疫疗法已经为某些类型的癌症带来了显著的效果,包括肿瘤缩小、生存率提高和缓解,甚至对那些对其他疗法没有反应的患者也是如此。然而,患者、肿瘤类型和治疗方法之间的反应率差异很大,只有一小部分患者对大多数治疗方法有反应。
例如,Javelin 100临床试验的最新结果,该试验将PD-L1抑制剂avelumab添加到头颈部癌症的放化疗中,没有显示出任何好处无进展或总生存期。即使在一个比较成功的免疫治疗试验中,Keynote-189对肺癌派姆单抗的研究,只有不到一半的患者对治疗有反应。
此外,接受免疫治疗的患者可能会出现严重的不良事件,特别是与其他治疗方法联合使用时。例如,近两倍的病人在激情130在晚期三阴性乳腺癌中的临床试验停用atezolizumab和nab-紫杉醇治疗与单独化疗比较。
虽然低级别免疫相关不良事件可以表明对治疗有反应,并且已经发生与提高生存率有关,这种免疫治疗的副作用需要仔细监测。
目前用于识别可能的应答者的方法是不够的
反应率的差异通常归因于癌症生理和患者潜在免疫系统的差异。因此,更好的患者画像可以帮助确定谁最有可能对给定的治疗做出反应,避免进行不必要的治疗,这种治疗可能弊大于利。
在某些情况下,使用基因筛查或蛋白质表达水平对患者进行分层提高了有效率。
例如,Keynote-001研究pembrolizumab在非小细胞肺癌(NSCLC)中的临床疗效表明,PD-L1表达在50%或更多肿瘤细胞中的初治患者的中位总生存期为34.9个月,而PD-L1表达低的肿瘤患者的中位总生存期为19.5个月。另一项研究表明PD-L1扩增NSCLC患者nivolumab的有效率为80%相比之下,没有这种症状的人只有不到20%。
然而,即使是最好的遗传生物标记物在临床实践中给出不同的结果。这些困难的出现是因为基因组和转录组并不总是代表完整的生物表型。
目前的分层策略也无法确定哪些患者可能经历严重的副作用,因此,不良事件仍然不可预测。
在蛋白质组中寻找免疫治疗生物标志物
除了传统的基因组学和转录组学方法,蛋白质组学的最新进展现在可以对潜在生物学进行更深入的研究,以搜索整个蛋白质组,以寻找免疫肿瘤学中的预测、预后和患者监测生物标志物。
下一代蛋白质组学技术,如数据独立采集(DIA)质谱分析方法由Biognosys,提供了一种无偏倚的方法来测量组织和生物流体(如血浆)的整个蛋白质组,具有前所未有的深度和规模。
因此,蛋白质组分析是一种很有前途的工具,可以揭示蛋白质组和治疗反应之间的关系,以便更好地筛选和分层患者。
将治疗前从患者收集的样本中的蛋白质特征与临床结果相关联,可以揭示相关的生物标志物,并建立可能对治疗有反应的患者的档案。
此外,在治疗期间收集更多的样本并跟踪蛋白质组的变化可以支持发现生物标志物,用于监测反应和管理免疫相关不良事件。
与免疫治疗反应和不良事件相关的生物标志物特征
对使用PD-1阻断剂治疗的非小细胞肺癌和黑色素瘤患者的概念验证研究证明了下一代蛋白质组学在发现预测反应和管理毒性的生物标志物方面的力量。
我N研究在2021年美国临床肿瘤学会的会议上发表,由Biognosys与黑素瘤研究人员Paolo A. Ascierto和国家肿瘤研究所IRCCS基金会的同事合作进行,组织样本取自抗pd -1疗法治疗前的晚期黑素瘤患者。
Biognosys将无偏性蛋白质组学分析与转录组学相结合,以鉴定与抗pd1疗法治疗的晚期黑色素瘤患者治疗反应相关的蛋白质和mRNA生物标志物。
该研究确定了64种与治疗反应相关的蛋白质和10种mRNA生物标志物候选物,提供了比单独的蛋白质组学或转录组学更全面的图像。
在进一步的研究中在2021年美国癌症研究协会会议上,研究人员将该分析中的蛋白质组学数据与临床结果信息结合起来。
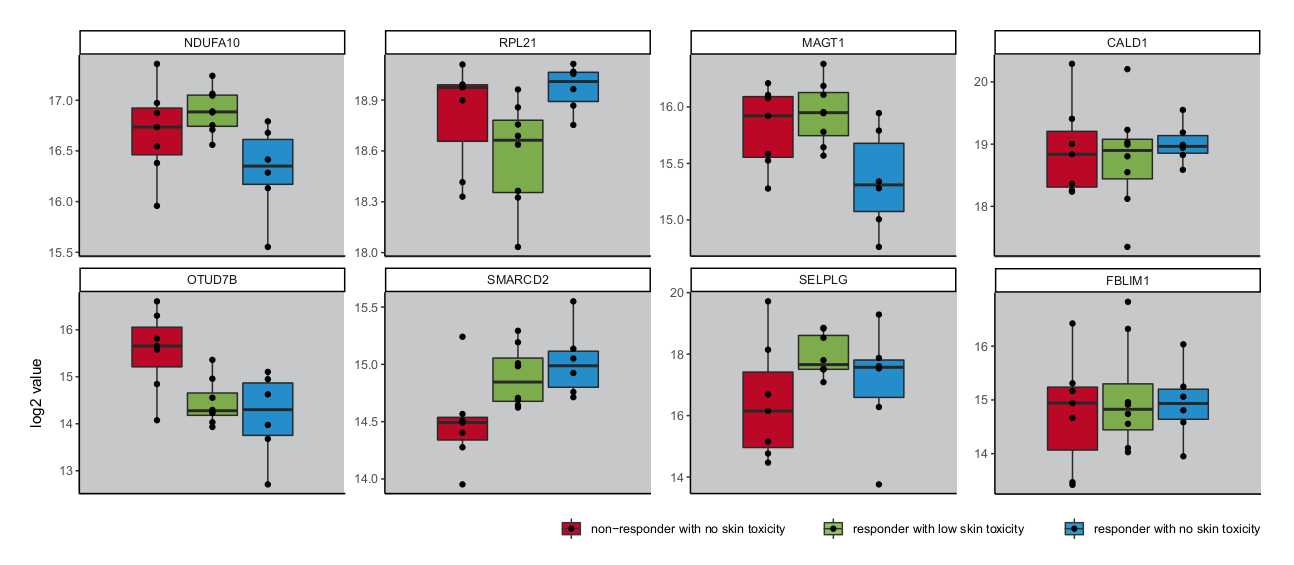
一组15个蛋白质被鉴定为预测治疗反应和毒性,与囊泡运输、代谢、炎症和免疫反应有关。在这15人中,有8人具有来自人类蛋白质图谱(参见图1).
在与Emanuela Romano及其在Curie研究所和San Luigi Gonzaga医院的同事合作中,Biognosys还使用抗pd -1免疫检查点抑制剂治疗前和治疗期间收集的血浆样本,检测了非小细胞肺癌患者的蛋白质组。
在2021年AACR会议,该团队确定了13种蛋白,它们在预测治疗反应和免疫相关不良事件方面显示出潜在的预后价值,代表了关键的生物学过程,包括急性免疫反应、脂质调节和糖基化。
下一代蛋白质组学不仅仅是识别生物标志物
综上所述,这些研究证明了下一代蛋白质组学在免疫治疗中识别新的预后生物标志物方面的力量。大规模、无偏的蛋白质组学技术可以通过将时间零点的蛋白质特征与临床测量值相匹配来识别几乎任何临床相关结果的预测性生物标志物。
但是深层蛋白质组学在免疫肿瘤学中的潜力还不止于此。
通过匹配肿瘤蛋白质组学特征与血浆蛋白质特征,可以将血浆和肿瘤生物标志物相关联,从而对患者进行微创监测,并消除频繁活检的需要。
此外,用下一代蛋白质组学补充药物发现工具箱中更传统的工具,如转录组学和基因组分析,可以全面了解患者的个人资料和对免疫治疗反应的可能性。
最后,无偏的蛋白质组学数据可以用于“反向翻译”,为潜在的治疗作用机制提供新的见解,并指出与现有或管道资产的新型组合策略,将使无应答者受益。
免疫肿瘤学领域的主要参与者越来越多地转向下一代蛋白质组学,以支持更好的患者分层,更成功的临床试验,最重要的是,为患者带来更有利的结果。

